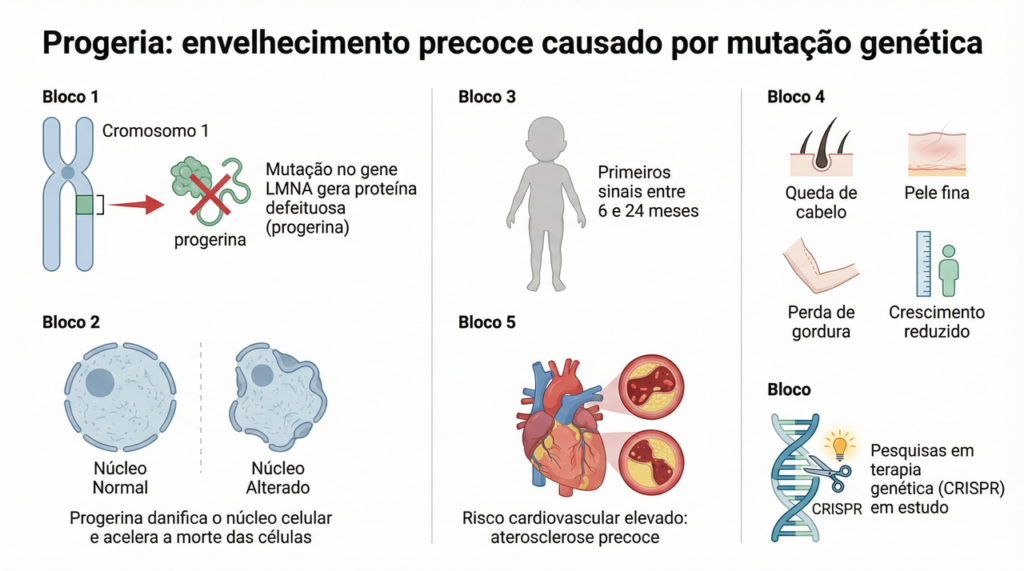
Progeria, também conhecida como síndrome de Hutchinson-Gilford, é uma síndrome genética rara que provoca envelhecimento extremamente acelerado em crianças, causado por mutação no gene LMNA. Essa alteração produz uma proteína anormal chamada progerina que danifica o núcleo celular, levando à morte precoce das células e manifestação de sintomas antes dos dois anos de idade.
Como uma mutação genética acelera o envelhecimento?
A síndrome de Hutchinson-Gilford resulta de mutação pontual no gene LMNA no cromossomo 1. Este gene codifica as proteínas lâmina A e lâmina C, componentes estruturais essenciais do envelope nuclear. Segundo publicação no PubMed, a mutação mais comum é c.1824C>T, responsável por aproximadamente 90% dos casos.
A mutação ativa um sítio de splicing incorreto, gerando a progerina com deleção de 50 aminoácidos. Essa proteína defeituosa acumula-se no envelope nuclear e desestabiliza o núcleo celular. O MedlinePlus Genetics explica que isso compromete funções vitais como replicação de DNA, expressão gênica e resposta ao estresse celular.
Quais sintomas aparecem primeiro nas crianças afetadas?
Bebês com progeria nascem aparentemente saudáveis e desenvolvem-se normalmente nos primeiros meses de vida. Os primeiros sinais surgem tipicamente entre 6 e 24 meses. Pesquisa publicada na base OMIM documenta que a falha no ganho de peso é o sintoma inicial mais frequente.
Características Físicas com Progressão Rápida
Alterações corporais observadas desde os primeiros anos de vida.
| Característica | Sistema afetado | Descrição clínica |
|---|---|---|
| Alterações capilares | Pele e anexos | Perda completa de cabelos, sobrancelhas e cílios, geralmente antes dos dois anos de idade. |
| Pele envelhecida | Sistema tegumentar | Pele fina, enrugada, com manchas visíveis e perda significativa de elasticidade. |
| Face característica | Estrutura facial | Olhos proeminentes, nariz fino em formato de bico e maxilar pequeno. |
| Lipodistrofia | Tecido adiposo e muscular | Perda severa de gordura subcutânea e redução importante da massa muscular. |
| Baixa estatura | Crescimento | Crescimento significativamente retardado desde a infância. |
Por que problemas cardiovasculares são a maior ameaça?
A aterosclerose acelerada representa a complicação mais grave da progeria. Artigo científico no PMC demonstra que crianças desenvolvem aterosclerose severa semelhante à de idosos, mas com características particulares. A perda de células musculares lisas nas artérias coronárias e aorta é a alteração mais importante.
Essas alterações causam rigidez arterial, calcificação vascular e formação de placas ateroscleróticas. Estudo no PubMed reporta idade média de óbito aos 12,6 anos por infarto ou AVC. O desenvolvimento cognitivo permanece normal, mas o coração falha precocemente.
Existem tratamentos que prolongam a sobrevida?
Não existe cura, mas tratamentos multidisciplinares melhoram a qualidade de vida e podem estender sobrevivência. Revisão científica no PubMed indica que a aspirina e estatinas reduzem risco cardiovascular através da prevenção de coágulos e controle do colesterol. Fisioterapia, nutrição especializada e acompanhamento cardiológico são essenciais.
Terapias complementares fundamentais:
- Fisioterapia regular: fortalece músculos e preserva mobilidade articular
- Nutrição especializada: compensa deficiências e mantém peso adequado
- Exercícios adaptados: melhoram circulação e função cardiovascular
- Monitoramento cardíaco: detecta precocemente complicações graves
- Órteses: corrigem deformidades ósseas e melhoram funcionalidade
Qual o futuro das pesquisas em terapia genética?
Avanços em edição genética oferecem esperança para tratamento definitivo. Pesquisadores investigam a tecnologia CRISPR/Cas9 para corrigir a mutação no gene LMNA ou silenciar a progerina. Artigo no PubMed descreve que essa tecnologia permite edição precisa do genoma, mostrando-se promissora para distúrbios genéticos.
Outras estratégias experimentais incluem inibidores de farnesilação, oligonucleotídeos antisense e microRNAs reguladores. Modelos murinos transgênicos testam eficácia antes de ensaios clínicos humanos. Embora nenhuma terapia genética esteja aprovada, resultados preliminares demonstram potencial real.









































